はじめに
米国脂質異常症の診療ガイドライン、実に8年ぶりのアップデート(2026・3・13公開)
丸1日半ぐらい、notebook LMの力を借りて、内容を把握しました。(私の「読む」という定義は何十年も前にみなさんの想像するものとは異なっています)
注意点
- ガイドラインの全てを網羅する解説を目指していない
- 変更点だけをピックアップしていない(過去のガイドラインにも書かれていたかもしれないが、今回気付いたものも含まれる)
- FH(家族性)については取り上げていない(しかしHeFH(ヘテロ)は意外と遭遇するので、対応できないといけない)
- 日本のもの、前回の米国のものの詳細はカバーしていない(対比のために概要だけ出している)
- あくまで、プライマリ・ケアの視点での脂質異常診療の観点からのまとめ(特に一次予防を重点的に)
- 脂質異常を扱う人間はプライマリ・ケアをやる以上一度は自分で目を通すべき(最初にある、10のTOP TAKE-HOME MESSAGESと、前回からの変更点、図表を見るだけでも)
- 考え方ではなく、とりあえずどうしたらいいの? という人は久我山ハートクリニックのページが極めてシンプルでわかりやすい。(でもここに書いているようなことは書いていません)
- これをそのまま日本で導入するべき、とは(今のところ)考えていない
まず前提:何を問うべきか
脂質診療の出発点は「LDLが高い人を見つけて下げること」ではない。プライマリ・ケアで問うべき臨床疑問は「この人の心血管リスクは心配するレベルか?」であり、その答えに応じて介入の有無と強度を決める、というスタンスに徹する必要がある。日本のガイドラインは一般社団法人 日本動脈硬化学会 (JAS)による動脈硬化性疾患予防ガイドライン 2022年版であり「脂質異常症」のガイドラインではないことを気づいている人はどのぐらいいるだろう? USPSTFの推奨も「Statin Use for the Primary Prevention of Cardiovascular Disease in Adults: US Preventive Services Task Force Recommendation Statement」と、心血管疾患の一次予防に関するスタチンの使用であり、「脂質異常症」の治療に関するスタチンの使用ではない。概ね他の国も同様の表現であり、そういう意味では米国が「Guideline on the Management of Dyslipidemia」と表現したのはある意味、異端児的と言える。
つまり健診などで脂質がひっかかった人が来た場合、他の心血管リスクに関する情報(年齢、喫煙、血圧、等代謝異常など)を踏まえずに、脂質の数字だけを見て治療する、しないを決断する医師はその本質を理解していない、と言っていい。
脂質異常症とスタチン適応はベン図のように多くは重なるが完全一致ではない。脂質異常がなくてもリスクが高くスタチン適応となる人もいれば、脂質異常があっても全体リスクが低くスタチン不要な人もいる。脂質値だけで「高いから治療」「正常だから放置」と決めると、治療すべき人を見逃し、治療不要な人に介入してしまうことになる。(治療薬の保険適応の問題は別)
岡田唯男 診療のプロが考える経済的負担を減らすための選択肢 ④脂質異常症 in 特集 所得格差時代の薬物治療. 薬局. 2018. Vol.69. No.5. 2244-2250
でまとめているし、予防医療四部作(特に2024年の「羅針盤」)でも詳しくまとめている。
世界的な本質は
個人のリスク計算(ざっくり低、中、高) → 治療閾値の判断(左に準じる) → 治療介入方法と目標(左に準じる)
であり、表にまとめると
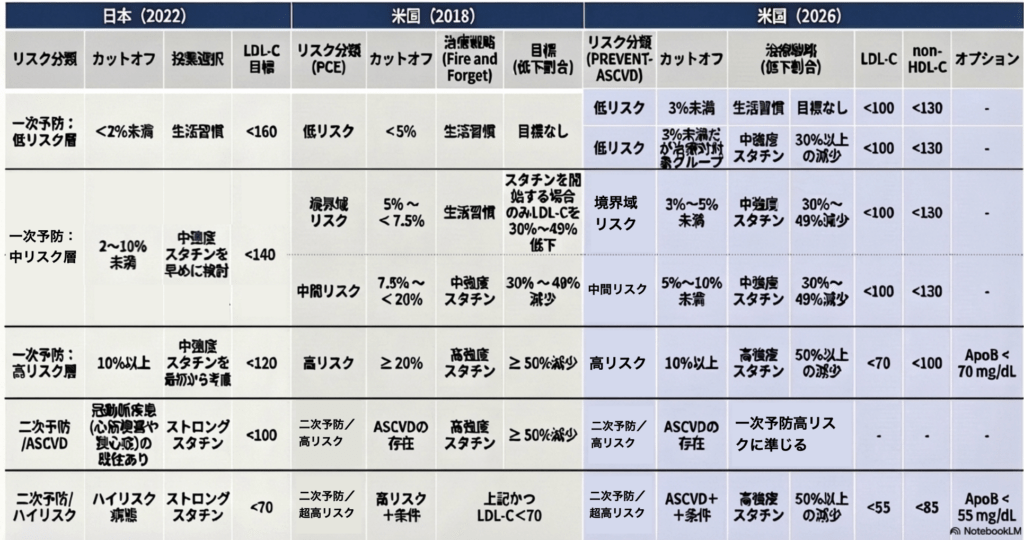
となるが(注:細かい例外、但し書きは表に含まれていない)、数字が国によって違う、とか覚えられない、という印象を持ってはならず、
個人のリスク計算(ざっくり低、中、高)
→ 治療閾値の判断(左に準じる) → 治療介入方法と目標(左に準じる)
の概念が、捉えられているかが重要で、繰り返すが、脂質異常症の基準を超える(一律の基準)から下げるという考え方は日本を含め世界の流れから外れている。
ただし
- リスク算出の方法
- 治療閾値のカットオフ
- 治療目標ややり方が異なる (fire and forget vs treat to target (減少割合での目標、LDLーCの目標))
が国によって異なり、そこが各国が「痒いところに手を届かせる」ために独自の工夫を凝らしているのだと言える
今回のガイドライン
表題に大量のアルファベットが並んでいる。なんと以下の11団体揃っての推奨
- ACC: American College of Cardiology
- AHA: American Heart Association
- AACVPR: American Association of Cardiovascular and Pulmonary Rehabilitation
- ABC: Association of Black Cardiologists
- ACPM: American College of Preventive Medicine
- ADA: American Diabetes Association
- AGS: American Geriatrics Society
- APhA: American Pharmacists Association
- ASPC: American Society for Preventive Cardiology
- NLA: National Lipid Association
- PCNA: Preventive Cardiovascular Nurses Association
気づく点としては
- AAFP(家庭医)、ACP(内科)は含まれていない
- 2026年版がこれら2018年の推奨を「引退させ、置き換える(retires and replaces)」ものであると明記(同意するかは別)
用語
- COR: class of recommendation。1, 2a, 2b, 3: no benefit, 3: harmがある。詳細についてはガイドライン参照
- LLT: lipid lowering therapy (薬物療法のこと。生活習慣の改善は含まない)
リスク評価の再構築
2026年ガイドラインの中心は、リスク計算式の刷新と、その上に組み立てられたCPRフレームワークにある。
PREVENT-ASCVD式【COR 1】
- 30歳から79歳までの既知のASCVDや明らかなサブクリニカル動脈硬化がない成人を対象とし、10年リスクだけでなく30年(生涯)リスクの推定も可能になった。
- 現代の集団(Contemporary Cohorts)データ: PCEが1970年代、1980年代、および1990年代に登録されたコホート研究(ARIC、CHS、CARDIA、Framingham研究など)の数十年前の古いデータに基づいていたのに対し、PREVENT™はより現代的で大規模な集団データ(論文はおそらく2024年)に基づく
- イベント率の低下: 現代では血圧管理や禁煙の普及、治療技術の向上により、同じ背景を持つ人でも数十年前に比べて心血管イベント(心筋梗塞や脳卒中)の発症率自体が低い。
- その結果、PREVENT™によるリスクスコアはPCEよりも40%〜50%低く算出される傾向。この低下に合わせて、治療を開始する「入り口」の数字も3%へと調整(後述)
- 年齢、性別、血圧(収縮期血圧および降圧薬の使用有無)、脂質値(総コレステロール、HDLコレステロール)、糖尿病の有無、喫煙習慣(30日以内に1本でも吸ったかどうか、と基準が明確)、腎機能(eGFR:推算糸球体濾過量)、スタチンの使用有無が必須。降圧薬やスタチンの使用の有無も入力で、考慮される。(この人スタチン飲んでるからTCがxxxだけど、飲んでない状態の数値じゃないとリスク判らないのでは? とか悩まない)
- オプションとして、HbA1c、尿中アルブミン/クレアチニン比、郵便番号(SDH的考慮!米国のみ)のわかるものだけでも入れるとより正確に算出
- 結果は10年リスクと30年リスクの両方が出る(30年リスクの使用法は後述)
- CVDリスク、ASCVDリスク、心不全リスクが見られる (画像下部参照)
- ASCVDリスク: 脂質管理用。脳卒中・心筋梗塞・冠動脈死の予測。(治療方針の決定にはこれを使う)
- 心不全リスク: 心不全発症の予測。BMIを追加して考慮。
- CVDリスク: 血圧管理用。上記2つの合算(完全な足し算ではないみたいです)

- 手計算で算出はできない。オンライン計算ツールはこちら
CPRフレームワークの導入【COR 1】
- C (Calculate): PREVENT™でリスクを算出。
- P (Personalize): リスク増強因子(CKM、家族歴、炎症疾患など)で個別化。
- R (Reclassify/Reassess): CACスコア等を用いてリスクを再分類し、治療を再考。
リスク分類のカットオフの再定義と累積暴露という概念の導入
- 一次予防: 低リスク(<3%)(これはさらにLLTを考慮すべき人とそれ以外に分ける)、境界域(3%〜5%未満)、中間リスク(5%〜10%未満)、高リスク(≥10%)の4群。
- 二次予防: 既往歴のある患者の大部分を「超高リスク(Very High Risk)」として定義(LDL-C目標 <55)。超高リスク: 既存の心血管疾患(ASCVD)があり、複数の重大なイベント歴がある、または1回のイベントと複数の高リスク条件(65歳以上、糖尿病、慢性腎臓病など)を持つ集団
- 早期からの累積曝露(Cumulative exposure)も考慮し30年リスクを見積もる。(低リスクに分類された場合にのみ、30年リスク(生涯リスク)が 10%以上かどうかを判断。後述)
CAC、Lp(a)、ApoB:残余リスクという考え方
PREVENT-ASCVDでリスクを算出して、リスクごとのLDL-Cを達成していても、PREVENT-ASCVDでのリスク算出に用いられなかった因子による「残余リスク」があれば、リスクを最小化できない、という立場。境界域〜中間リスクの患者で「スタチンを始めるかどうか迷う」場面で、ガイドラインはCAC、Lp(a)、ApoBを積極的に使うことを推奨している。
- Lp(a)測定: 全成人に生涯に1回の測定を推奨 【COR 1】
- CACスコア: 治療開始に迷う境界域・中間リスク者での再分類に使用 【COR 1】。
- 分類: 0(なし)、1-9(極軽度)、10-99(軽度)、100-299(中等度)、300-999(重度)、≥1000(広範)。
- 0:リスク組み替えにより多くでスタチン延期も検討可。
- 300以上、あるいは一部では100以上二次予防相当のハイリスクとみなす。
- ApoB測定: 脂質低下療法(LLT)中の治療強化の判断材料として推奨 【COR 2a】。
- hsCRP: 境界域リスクで治療開始を検討する際の指標(2回連続で≥2 mg/Lの場合、高強度スタチンが有益) 【COR 2a】 (日本では自費検査です)
LDL-C推定式の変更:Friedewald式から新式へ 【COR 1】
- Martin/Hopkins式またはSampson/NIH式の使用を強く推奨(これも手計算ができない。オンラインなどの自動計算のページが必要)
- 直接測定法よりもこれらによる推定値を優先する立場(超遠心法を除く)。
- 非空腹時やTGが高値、LDL-Cが極低値の場合でも高い精度を維持。
治療方針の考え方:目標値管理(Treat-to-Target)の復権と強化
今回のガイドラインは、スタチン強度だけを決めてあとは「打ちっぱなし(fire and forget)」ではなく、%減少と具体的な目標値の両方を追う「treat-to-target」を明確に再導入している。
管理目標値(Treat-to-Target)の本格復帰
- 目標値はベースラインからの%減少、LDL-C目標値、non-HDL-C目標値の3つが示されている。
- 可能な限り全て達成が望ましい、が優先順位としては、
- ベースラインからの%減少:「すべての個人において引き続き優先事項(remains a priority)」とされる(多くの大規模臨床試験において、心血管イベントの抑制効果が、LDL-Cを「何%下げたか」という減少の大きさに相関していることが証明されているため)(%減少は数値目標を設定していなかった2018のガイドラインでも言われていました)
- 数値目標:たとえ%減少を達成していても、LDL-Cが依然として目標値(例えば100 mg/dL)以上の場合は、治療の強化(スタチンの増量や他剤の追加)を検討するための具体的なトリガー(閾値)として機能
- non-HDL-C:LDLだけでなく「すべての動脈硬化誘発性リポタンパク質」に含まれるコレステロールを反映。特にトリグリセリド(TG)が 150 mg/dL 以上の場合や、肥満・糖尿病などがある場合、LDL-Cだけでは動脈硬化リスクを過小評価する可能性があるため、この指標を達成することを重視
Lower is Better(低ければ低いほど良い)の原則
- LDL-Cが極めて低いレベル(30mg/dL以下など)に達しても、追加のリスク低減が認められ、長期の安全性も確認された。(らしい。要確認)
治療閾値の考え方
ガイドラインでは、薬物療法を開始するかどうかの判断基準として「正味の臨床的利益(ベネフィット - 潜在的な害)」という考え方を用いている。(正味利益はUSPSTFのところでも重要な基本概念)
- ベネフィットの指標: 1件の重大なASCVDイベント(心筋梗塞、脳卒中など)を防ぐために必要な治療人数(NNT-benefit)
- 害(ハーム)の指標: スタチン治療の結果、1件の新規糖尿病を発症させるのに必要な人数(NNH または NND: Number Needed to Harm / Damage)
- 注:糖尿病は、スタチンによる最も一般的で深刻な副作用、かつ高強度スタチンの方が糖尿病発症のリスクが高い
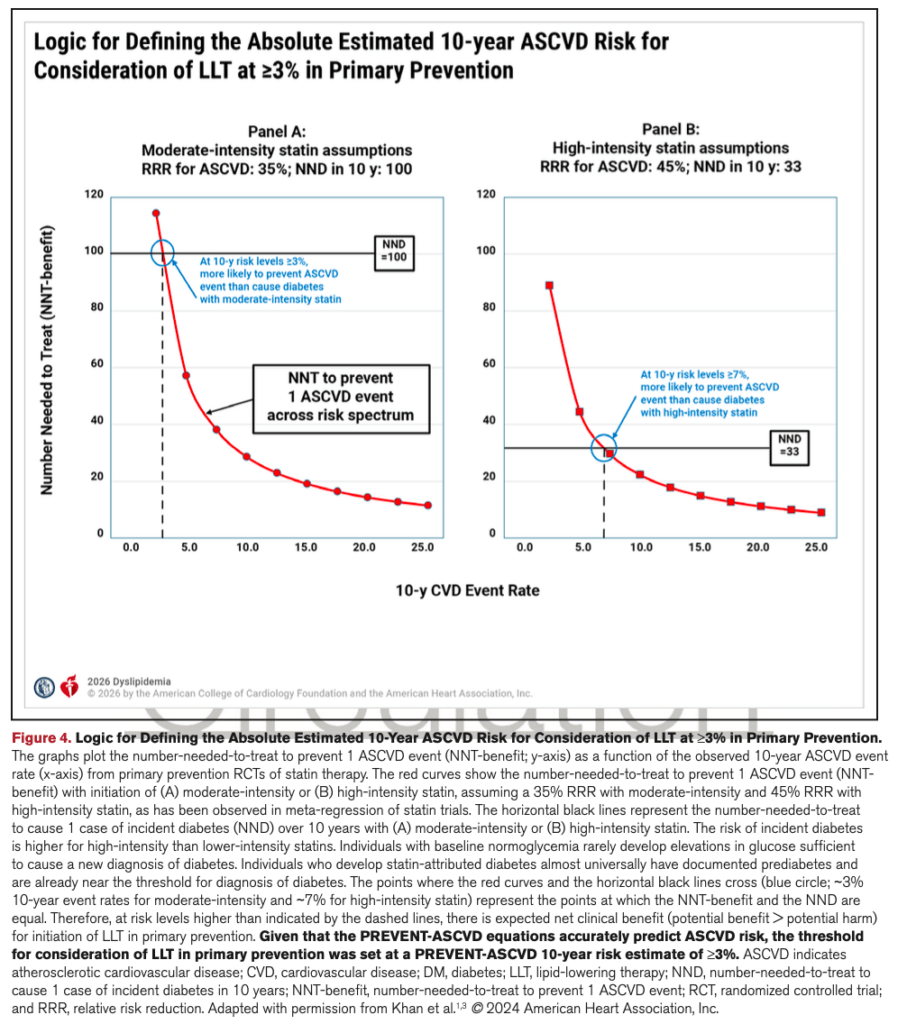
Figure 4が示す「拮抗点」の正体
Figure 4のグラフ(Panel A:中強度スタチン)では、
中強度スタチンの場合: 10年間で1件の糖尿病を発症させる人数(NND)は100人。
交差するポイント: グラフ上で「1件のイベントを防ぐための人数(NNT)」の曲線と、この「NND = 100」の水平線が交差する点が、まさに10年リスク 3% の位置になります
論理的結論: 10年リスクが3%以上の集団では、「イベントを1件防ぐために必要な人数」が100人以下になります。つまり、「1人の糖尿病を発症させるリスクを冒す間に、1人以上の心血管イベントを防ぐことができる」状態となり、潜在的な害よりもベネフィットが上回る(ベネフィット > ハーム)と判断されます
Panel B: 高強度スタチンの場合、NNDが33(!)のためNNT <33のレベルでないと1人のイベントを防ぐより先に糖尿病の発症を増やすため。リスクとベネフィットの拮抗点が10年リスク7%。
これは中間リスク(5〜10%)のちょうど真ん中あたり。最初の表では中間リスクは中強度スタチン、LDL-C30%以上の減少となっているが、その後に「for those in the higher end of this risk range, a high-intensity statin is beneficial to further reduce LDL−C by≥50(このグループのリスクの高い方よりの人たちは高強度スタチンでLDL-C50%以上で利益が得られる 【COR 1】」の記述あり。ということで中間リスクはさらに2群に分ける方が良いかもしれない。
治療目標の引き下げ(強化)
一次予防
- PREVENT™で算出された10年リスク ≥3%(境界域リスク以上)から、LLTの開始を医師と患者で対話(SDM)し検討できる 【COR 2a】。
- 境界域リスク (3%〜5%未満) :検討できる(can be considered)【COR 2a】
- 中間リスク (5%〜10%未満): 検討すべき(should be considered) 【COR 1】少なくとも中強度のスタチン治療(前述の通りこの中でもリスクが高い方寄りは高強度を検討)
- 高リスク (10%以上): 強力な脂質低下療法が推奨 【COR 1】高強度スタチン
- 低リスク(3%未満)での例外的な推奨: 10年リスクが3%未満(低リスク)でも以下のいずれかを持つ30歳〜59歳の成人では中強度スタチンの開始が合理的【COR 2a】:
- LDL-Cが160〜189 mg/dL と持続的に高い場合(二次性を除外し、4〜12週間程度生活習慣の改善を行なってもなお複数回の測定時で持続)
- 30年リスク(生涯リスク)が 10%以上 と算出された場合(ここで30年リスク(累積リスク)を使う)
- リスク計算値に依存しない「無条件一次予防LLT」群
- 糖尿病患者 (40歳〜75歳): 中リスクとして対応【COR 1】、複数のASCVDリスク因子がある場合は高リスクとしての対応が合理的【COR 2a】
- 慢性腎臓病 (CKD ステージ3または4) 患者: 中リスクとして対応【COR 1】
- HIV感染者 (40歳〜75歳)(安定した多剤併用抗レトロウイルス療法を受けている場合): 中リスクとして対応【COR 1】ただし臨床試験(REPRIEVE)では、薬物相互作用の少ないピタバスタチン 4mg(中強度)の有効性
- 重症高コレステロール血症 (LDL-C ≥190 mg/dL): 最大耐容量のスタチン療法(原則として高強度スタチン)【COR 1】ただし目標値は中リスクと同じ
- 目標値
- LDL-C<130は廃止
- 低リスクで、LLTの対象にならない場合:であっても、LDL-C<100 、non-HDL-C<130 mg/dL 未満(%減少の目標なし)が「一般集団における最適(optimal)なレベル」と位置づけ。【COR 1】たとえ低リスクであっても、これらの目標値を超える状態が長期間続くことは、動脈硬化性リポタンパク質への「生涯にわたる累積曝露(Cumulative exposure)」を増やし、将来のリスクを高める原因となるため、生活習慣の改善によってこのレベルを維持することを重要視。
- 10年リスクが3%未満(低リスク)であっても脂質低下療法(LLT)を考慮するグループ:中強度スタチン、%減少>30%、LDL-C<100、non-HDL-C <130 全て【COR 2a】
- 境界域リスク:中強度スタチン、%減少 30%〜49% 、LDL-C<100、non-HDL-C <130 全て【COR 2a】
- 中リスクの低い方(7%未満)まで:中強度スタチン【COR 1】、%減少 30%〜49% 【COR 1】、LDL-C<100、non-HDL-C <130の目標は合理的【COR 2a】
- 中リスクの高い方:高強度スタチン、 50%以上 減少【COR 1】,数値目標なし?
- 高リスク:高強度スタチン、 50%以上 減少【COR 1】LDL-C<70、non-HDL-C <100の目標、目標未達時のエゼチミブ追加は合理的【COR 2a】
- 高リスクでLDL-C<55を目指すべき特例:CACスコア ≥1000 AU の集団【COR 1】(このレベルの石灰化がある人は、二次予防の安定期にある患者と同等のリスク(年間死亡率など))、CACスコア 300〜999 AU の集団 【COR 2a】
- ややこしそうだが、まとめると一次予防は目標 は3種類 (%減少50%以上/LDL<70/non-HDL<100の高リスク群 またはそれ以外の %減少30〜49%/LDL<100/non-HDL<130、例外的にLDL-C<55)、介入も原則3種類(だが、それをやれば良い、というのではなく、数値目標達成が重要)(生活習慣のみ、中強度スタチン、高強度スタチン(7%以上))に集約される
二次予防
- 超高リスク群以外(高リスク):高強度スタチン、50%以上減少、LDL-C <70、non-HDL-C<100全て【COR 1】、スタチン単独で <70 / <100 未達時、エゼチミブ、PCSK9 mAb、ベンペド酸の追加【COR 2a】、医師の判断や患者の意向により LDL-C <55 / non-HDL-C <85 を目指す【COR 2a】
- 超高リスク::高強度スタチン、50%以上減少、LDL-C <55、non-HDL-C<85、最大耐容量のスタチンで目標未達時、エゼチミブ または PCSK9モノクローナル抗体 を追加、全て【COR 1】オプションとして ApoB <55 mg/dL、ベムペド酸 または インクリシラン(PCSK9 mAb不耐容時など)の追加【COR 2a】
- 超高リスクの定義:下記のどちらか
- 重大なASCVDイベントの既往が2回以上(例:12ヶ月以内の急性冠症候群、心筋梗塞、脳梗塞、症状のある末梢動脈疾患)
- 1つの重大なイベント既往に加え、複数の高リスク特徴がある(65歳以上、糖尿病、喫煙、高血圧、心不全、慢性腎臓病、最大耐容量の治療下でLDL-C ≥100 mg/dL)
- 特別な病態
- 慢性腎臓病(CKD ステージ3以上)合併時: ASCVD既往がある場合、高強度スタチン(±エゼチミブ/PCSK9 mAb)により LDL-C <55 / non-HDL-C <85 を達成することが強く推奨【COR 1】
- Lp(a)高値合併時: 目標未達成の場合、心血管ベネフィットが証明された PCSK9 mAb の追加が推奨されます【COR 1】
- 持続的な高TG(150-499 mg/dL)合併時: スタチンによりLDL-C目標を達成した後、イコサペント酸エチル(IPE) の追加が検討されます【COR 2a】
超高リスクの目標引き下げ(<55)はやりすぎか?
超高リスク群のLDL-C目標値が55mg/dL未満に引き下げられた根拠は、「低ければ低いほど良い(Lower is better)」という概念が大規模な介入研究によって科学的に証明されたことにある。
メタ解析では、LDL-Cが77mg/dL未満の低値からさらに約39mg/dL低下させるごとにASCVDリスクが21%減少することが示されている(らしい)。
具体的には、スタチンに非スタチン製剤を追加したIMPROVE-IT(達成中央値53mg/dL)、FOURIER(同30mg/dL)、ODYSSEY OUTCOMES(同40mg/dL)といった試験において、LDL-Cを極めて低いレベルまで下げることによる有意なイベント抑制効果が確認された。
さらに、LDL-Cが20mg/dL未満に達した層でも段階的なリスク減少が認められる一方で、FOURIER-OLE試験では中央値30mg/dLという超低値を8年間維持しても安全面に問題がないことが報告されている。
これらの知見に基づき、エゼチミブやPCSK9阻害薬の安全性と普及を背景として、超高リスク患者が享受できるベネフィットを最大化するために目標値が従来の70から55へと刷新されたのである。
(おそらく、前述の3試験の中で、それらの試験の結果を担保するために、せめて最も達成中央値が高かった53mg/dLまでは目指しましょう、ということなのだろう。)
治療薬について
ここは簡単に。
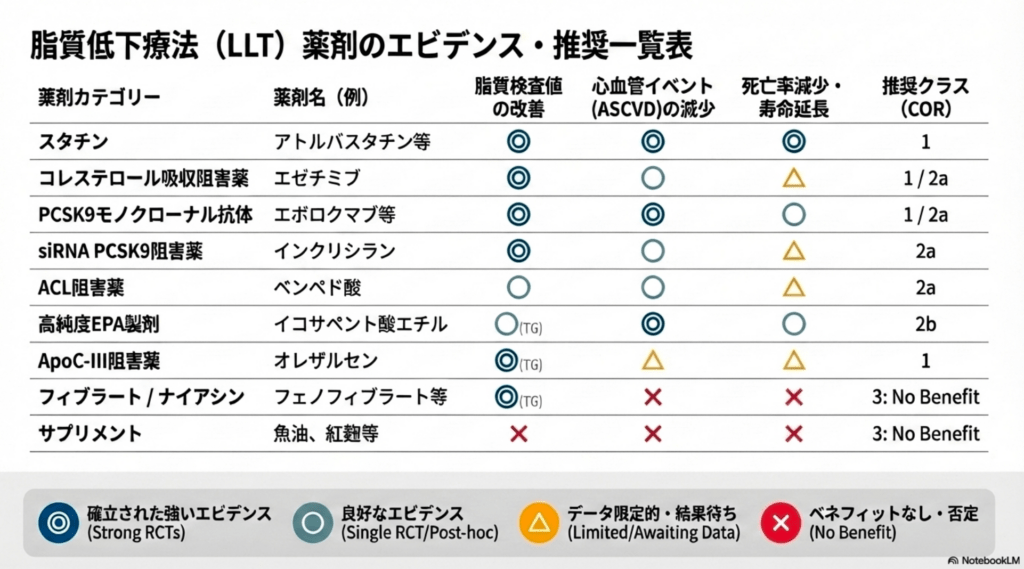
以下のエントリーを踏まえて上記画像を眺めたら、選択すべき薬剤は自明。(長生きできる薬は基本一種類のみ。スタチンなしで、それ以外の薬しか使われていない患者さんの主治医の処方ロジックを聞いてみたいです。)
サプリメントは「COR 3: No Benefit」
今回のガイドラインで目を引くのは、いわゆる「心血管サプリ」へのかなり強い否定的スタンスだ。SPORT試験では、低用量ロスバスタチン5 mgと、以下のサプリメントを比較した。
魚油 (Fish oil)、シナモン (Cinnamon)、ニンニク (Garlic)、クルクミン/ターメリック (Curcumin / Turmeric)、植物ステロール (Plant sterols)、紅麹 (Red yeast rice)、
結果として、ロスバスタチンはLDL-Cを約35%低下させたのに対し、いずれのサプリメントもLDL-Cをプラセボより有意に下げなかった。 有効性だけでなく、一部サプリで不利な変化もみられたことから、ガイドラインはLDLやTG低下目的のサプリ使用を「COR 3: No Benefit」とし、推奨しない立場を明確にしている。
それ以外に推奨しないものとしてバーベリン (Berberine)、また、スタチン関連筋症状(SAMS)に対するコエンザイムQ10も、ルーチン使用は推奨されない(COR 3)とされた。
その他
CKM症候群という新しい枠組み
今回のガイドラインは、単なる脂質ガイドラインではなく、CKM(Cardiovascular–Kidney–Metabolic)症候群という新しい概念に明確に足場を置いている。
CKM概念が必要とされた背景には、3つの知見がある。
- ① 腎臓の心血管リスク媒介機能の再認識:CKDが代謝リスク因子と心血管疾患(特に心不全)の双方向的関係を増幅する独立したメディエーターであることが明確化された。MetSはこの心腎相関を構造的に無視していた。
- ② 新規薬剤クラスの登場:SGLT2阻害薬とGLP-1受容体作動薬が心臓・腎臓・代謝の3領域にまたがる多臓器保護効果を示したことで、臓器横断的な疾患概念と治療戦略の整合性が求められるようになった。 SGLT2阻害薬はHF入院抑制・CKD進行抑制、GLP-1RAは体重減少・MACE(主要心血管イベント)低下において補完的な効果を示す。
- ③ 心血管疾患死亡率のプラトー化:50年にわたり改善してきたCVD死亡率が近年鈍化・一部で上昇に転じており、従来の危険因子管理の枠組みだけでは不十分であることが示された。
これらを踏まえ、AHA Writing Committeeのchair、Johns Hopkins大学のChiadi E. Ndumeleらは2023年のCirculation誌掲載の会長勧告において「心血管疾患リスク、予防、管理の再定義」を提唱し、CKMを初めて正式に定義。
Ndumele CE, et al. Cardiovascular-Kidney-Metabolic Health: A Presidential Advisory From the American Heart Association. Circulation. 2023;148(20):1606-1635.
CKMはステージ0〜4の連続体として定義され、肥満・糖代謝異常・CKD・CVDを包括的に評価し、社会的決定要因も組み込んだ形で管理していく枠組みである。(想像以上に多くの人がCKMに含まれる!)
リスク増強因子(Risk Enhancer)としての認識【COR 2a】、ApoBの測定推奨【COR 2a】、管理栄養士(RDN)への紹介推奨【COR 2a】
また、欧州動脈硬化学会は、肝(MASLD)も明示的に包含するSystemic Metabolic Disorder(SMD)概念を打ち出しており、CKMとの補完関係が議論されている。
日本人(東アジア人)への注意点
ガイドラインは人種・民族差にも言及しており、日本人を含む東アジア系ではスタチン(特にロスバスタチン)の血中濃度が高くなりやすく、有害事象リスクが相対的に高い可能性があると注意喚起している。 そのため、低用量から開始し、忍容性と効果をみながら漸増するアプローチが推奨されている。
わかっていないこと(調べきれていないこと)
1)リスク計算:Prevent式が日本人でも正確にリスクを見積もれるのか? (やはり久山町スコアが良さそう)
2)LDL-Cの推定:日本人でもMartin/Hopkins式またはSampson/NIH式 で良いのか
3)治療閾値のカットオフ:日本人での中強度スタチン、高強度スタチンの糖尿病発生リスク(NNH)が幾つで、治療のNNTがいくつで、拮抗点となる10年リスクは何%か? (ここがはっきりしないと誰にどのスタチンを入れるべきか決められない)
4)治療目標値:日本人でもLower the betterなのか?%減少やLDL-Cの目標値はどのぐらいがいいのか(日本の2022のガイドライン通りで良いのか)
特に治療閾値に関しては、スタチンによる糖尿病発症リスクとは別に、
- Smith GD et al. (BMJ 1993): 低リスク群での脂質低下療法は総死亡がOR 1.22(95%CI 1.06–1.42)と有意に増加した 。
- CTT 2012 (Lancet): 低リスク群(5年血管イベントリスク<10%)では死亡の増加はなかったものの,脂質低下療法の本来の目的である心血管イベントの低下効果そのものが認められていない
を中心に、「低リスクではネット・ベネフィットが乏しい」と支持する研究と、「低~中間リスクにもベネフィットあり」とする研究がそれぞれ多数あり、まとめて解析し結論を出そうとすると気が遠くなるレベル(しかし利益ありの方が論文数は多い)で、一度調査したが、やる気が削がれてしまっている。
本ガイドラインをどう位置づけるか(プライマリ・ケアの視点)
このブログの目的は、2026 ACC/AHAガイドラインの全訳や網羅的レビューではない。プライマリ・ケアで一次予防を考えるときの「考え方の枠組み」を整理することにある。
- 脂質値ありきではなく、リスクありき
- リスク評価をなるべく正確に
- リスクグループがわかり、介入すると決めたら、「何%下げるか」と「どのレベルまで下げるか」をセットで考える
- サプリよりスタチン、というメッセージはかなり明確
上記「わかっていないこと」の1〜4については個人的に調べ始めているが、まだ今回のガイドラインを日本人にそのまま当てはめるのは、時期尚早で、これを踏まえての日本の研究や考察、ガイドラインのアップデートを待つのが良いかもしれない。日本にそのまま導入すべきかについては、少なくとも現時点で私は「様子見」寄りである。とはいえ、リスクベースの考え方、累積曝露、CKMという枠組み自体は、今後の日本のガイドライン改訂を考える上でも避けて通れないだろう。
ここまで




コメント