はじめに
これは仮定に仮定を積み重ねたフェルミ推定である。突拍子もない結論に見えるかもしれないが、一応ロジックの積み重ねでそこに至っている。かなり深掘りをしているので、的外れな議論はしていないはずだが、学術的な自信があるならブログではなく学術誌に投稿している訳なので、こちらに公開している、という点も汲んでもらいたい。
本稿では一次予防をメインに扱い、二次予防については割愛する。また、極めて長文であることをあらかじめ断っておく。
御三家(高血圧・糖尿病・脂質異常症)に限らず、慢性疾患の中で「正しい」診療をするのに最も困難な領域は脂質異常症だと考えている(脂質異常症をちょろいと考えている人は、10回ぐらい考え直してほしい)。
おそらく大半の人が、読む途中でどうでも良くなり認知的降伏(cognitive surrender)を起こすと思う。それに負けず、最後まで読んだとしても、「脂質異常症とスタチンの適切な使い方がいかに難しいかが良くわかる」だけで、「どう使えば良いか結局わからない」ということになると思う。
だから、めんどくさいから結局日本のガイドライン通りでいいのでは? というのはある意味正しいスタンスなのかもしれない。
日本と米国のガイドラインの推奨から見え隠れする「スタンス」「考え方」の違いを列挙し、どちらにどのくらい寄せて診療するかを論じていく。
急いで答えの欲しい人は、「私案」でよければ、自分なりの提案をしているので「結局どうすれば良いのか?」の部分を読んでいただければ。
このエントリー作成に相当の資料、論文分析と思考時間を費やしている。引用の際は適切にお願いしたい。
日米ガイドラインの基本的な共通枠組み
個人のリスク計算(ざっくり低・中・高)→ 治療閾値の判断 → 治療介入方法と目標、という流れは日米共通である。
しかし以下の点が異なる。
- リスク算出の方法
- 治療閾値のカットオフ
- 治療目標とやり方(fire and forget vs treat to target、LDL-C減少割合での目標 vs LDL-C数値目標)
米国ガイドラインの概要については前稿を参照されたい。
ガイドラインの「呼び名」
世界のガイドラインの多くは「動脈硬化性疾患の予防に関するガイドライン」という呼び名であり、日本はそれに沿っている。一方、米国は「脂質異常症のガイドライン」という呼び名を採用している。この点は上記エントリー参照
しかし中身を見ると、タイトルとは逆に日本は脂質を下げることが中心であり、米国はリスクを下げるためのスタチンの使い方がメインである(あえて違いをはっきりさせるならば)。
日米の有病率・罹患率の違い
日本では久山町スコア、米国では2018年ガイドラインのリスク計算に用いられたPCE(Pooled Cohort Equations)および現行のPREVENT式の研究から、以下のような数値が示されている。
日本(久山町研究) 粗ASCVD発症率:5.8/1,000人年、10年リスク換算で約3%(Supplemental Table 1)
米国(PCE — PREVENTの前身) 全体の粗発症率:16.89/1,000人年(累積発症率3.6%、最長10.65年追跡の米国一般集団サンプル)
典型的な10年ASCVD推計値(米国成人・中年)
- PCE(2013):中央値 7.1〜16.0%(集団・年齢による)
- PREVENT(2023):中央値 約5〜7.7%
PCEの時代からかなり改善しているとしても、粗発症率で5.8/1,000人年 対 16.89/1,000人年というのは3倍の開きである。スタチンの発症率抑制の割合が同じでも、NNTが異なってくる(それに伴い治療閾値も変わる。後述)。
Honda T, Chen S, Hata J, et al. Development and Validation of a Risk Prediction Model for Atherosclerotic Cardiovascular Disease in Japanese Adults: The Hisayama Study. J Atheroscler Thromb. 2022;29:345–361.
こうした背景もあり、日本ガイドライン(2022)には以下のような記述が各所に見られる。
「わが国における冠動脈疾患の絶対リスク(発症率や死亡率)は、現時点では欧米に比べるときわめて少ない」(第2章 1.1)
「これら(米国の推奨)は日本人に比較し冠動脈疾患の多い欧米人集団を対象にした研究がその根拠の中心になっており、日本人にそのまま当てはめるのは不適切であろう」(第2章 1.12:BQ10)
「米国(ACC/AHA 2018)では絶対リスク20%以上をハイリスクとしているのに対し、日本(JAS 2022)では10%以上をハイリスクと設定しており、これら基準の設定は、国ごとの動脈硬化性心血管疾患の発症率・死亡率や集団寄与危険割合の違いにも影響を受けることから同等に比較はできない」(第3章 1.2)
また米国(2026)でも以下のように述べられている。
「特定集団のサンプルに対してリスク予測モデルの再校正(recalibration)を行わずにルーチンで実施すべきではない。それは、患者の系統的な誤分類(systematic misclassification)を引き起こす可能性があるからである」
この点は、後述する拮抗点の推定に関連してくる。
リスク見積もり方法の違い
米国(2026)はPREVENT-ASCVDでより正確な見積もりとなった。同様に日本(2022)も久山町スコアでより正確・望ましいとされた。
どちらが望ましいというより、自国民のイベント発症率をいかに正確に推定するかが治療対象者の同定に極めて重要であるため、日本人には久山町スコアを、米国人にはPREVENT-ASCVDというのが正解である(追って余裕があれば推定値のずれを検証予定)。
久山町スコアについてのいくつかのトリビア
久山町スコアについては計算ツールや計算表しか見たことがない人も多いだろう。原著では「8項目27点満点スコア」「80〜84歳までリスクが計算できる」だったのが、ガイドライン版では「6項目19点」「リスク計算は79歳まで」に変更されている(蛋白尿と運動習慣をリスク算定評価項目から除外)。
ガイドライン(P68〜70)では変更理由が以下のように説明されている。
「なお75歳以上でも日本人の脂質低下療法による心血管イベントの抑制効果が報告されている(第7章「高齢者」参照)。しかしながら高齢になると年齢そのもので絶対リスクが跳ね上がること、合併症の状態など個人差が大きいことなどから、80歳以上の後期高齢者の一次予防に関しては、スコアの結果をただちに管理目標値に紐づけるのではなく、患者の状態を把握して個別の治療を行うべきであると考えられるためフローチャートには入れていない。」
「これら6項目は、現在地域で行われている特定健診、あるいは職域での定期健康診断において検査として含まれている項目であり、汎用性が高いと考えられた。」
「オリジナルのスコアには、糖尿病とCKDの指標であるタンパク尿が危険因子として選択されていたが、本ガイドラインでは、糖尿病とCKDが存在すれば(その時点ですでに)高リスク病態であるため、脂質管理目標を定めるための絶対リスクを予測する項目からは除外した。」
「同様にオリジナルの久山町スコアは、運動習慣の有無が含まれているが、日常診療で常に情報を聴取していない可能性があるため本ガイドラインでは使用しない。」
しかしながらこのように「開発」されたガイドライン用スコアの予測性能について検証された論文は存在しない。
さらに、スコアの限界についても以下の記述がある。
「久山町スコア開発の過程において降圧薬の有無は最終モデルに残らなかった。またその他の服薬については欧米のガイドラインと同様に考慮されていない。一般的に同じ血圧レベルの場合、降圧薬服薬者の方が、非服薬者に比べて脳卒中の絶対リスクは高くなることが報告されているため、モデルに残らなかったとはいえ降圧薬服薬者では絶対リスクが過小評価される可能性を考えるべきである。この議論は、2017年版の吹田スコアを採用した際にも行われており、服薬者に対して絶対リスクの評価を行う場合には考慮すべき事項と考えられた。」
「脳・心血管疾患発症率には、前述のように地域差や社会的要因による差があることが指摘されている。したがって、絶対リスクを評価する際にはそのような要因を考慮する必要がある。……2022年版のリスクスコアは、久山町研究のデータから作成されたものであり、絶対リスクの国民集団として代表性があるとは考えにくい。……本来は2012年版のNIPPON DATA80のように日本国民から層化無作為抽出された集団で検討するのが理想であるが、その場合は発症調査ができないという現状があり、今後の検討課題である。」
日本人のリスク推定の公式ツールはNIPPON DATA80 → 吹田スコア → 久山町スコアと移ってきており、久山町スコアが理論的には現在のベストではあるが、それでも特定のコホートに基づく推定であることから完全ではないことが示されている。
その後、以下の外部検証が行われた。
Honda T, et al. External Validation of a Risk Prediction Model for Atherosclerotic Cardiovascular Diseases in a Large National Health-Checkup and Claim Database. J Am Heart Assoc. 2025;14(16):e040386
無作為集団ではなく特定健診受診者コホートではあるが、特定健診+レセプトデータ420,552人・40〜74歳・中央値4.4年追跡にて、「オリジナルの」久山町スコア(8項目版)が検証された。相対リスク(誰が高リスクか)はよく当たるが、特定健診受診者では絶対リスクをやや高めに出すことが判明している。(この論文で運動習慣の欠測率(データなし)が最大で20.1%であった、というこということもありガイドライン用スコアからこの項目を外す理由としては妥当(だが検証して欲しかった))
なお参考として、米国の最新ガイドライン(2026年版 ACC/AHA)においてPREVENT™計算式の基盤となったのは合計660万人規模のデータセットである。
一方、久山町スコアの開発に用いられた対象集団は、心血管疾患既往のない40〜84歳の日本人たったの2,454人で、24年間の追跡期間中に270人が最初のASCVDイベントを発症している。
重要な論点:ガイドラインにおいて「ガイドライン版」久山町スコアが作成されており、項目や対象の変更理由は明記されているが、オリジナル版との予測性能や一致度が同じかどうかについて検証された論文は存在しない(と思われる。AIのdeep researchでも存在しないという回答)。また、外的妥当性の評価をしたHondaらの研究もオリジナルの8項目版の検証である。これは重大な論理の飛躍である。日本人のリスク推定は久山町スコアが現状のベストと考えられるが、運用のしやすさを優先してガイドライン版(というオリジナルの推定方法)を設定したために、オリジナル版と同じレベルの予測性能があるかはわからない。(この検証の研究があればお知らせいただきたい)
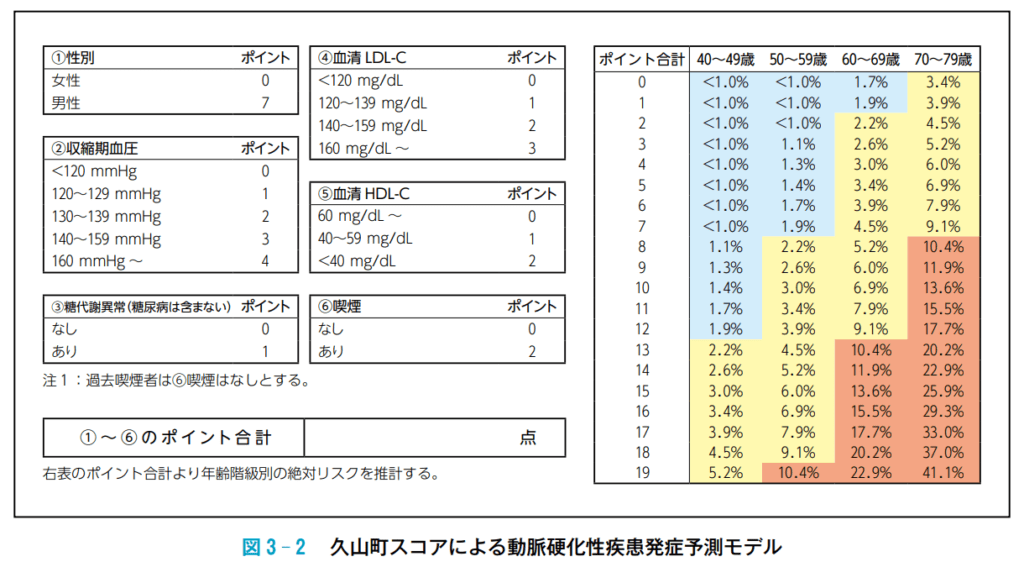
久山町スコアはアプリで計算しない(ことを推奨)
久山町スコアは日常的に計算しているが、公式のアプリや自動計算機(リスク算出)は使用していない。下記の実際の算出用テンプレートを印刷し、患者さんと一緒に確認して、それぞれの該当ポイントに丸をつけながら、算出する。(そのままカルテにスキャナ取り込み)
理由:
- 本エントリーの主題である、リスク算出はまあ正しいとしても、リスク分類(低、中、高)やLDL-Cの治療目標がガイドライン通りでは適切でない可能性が高い アプリや計算機は結論(リスク分類と目標)だけが出力される こちらとしては素点のポイント合計だけあれば良いのに、それが出力されない
- 患者さんと一緒につけることで、丁寧な説明につながる、また脂質や血圧が下がったり、タバコを止めることで、何ポイント減って、リスクグループがどのように変わるか視覚的に説明できる
スタチンの分類の違い
これは米国(2018)の時からわかっていたことだが、「スタンダードスタチン」「ストロングスタチン」は、米国の「中強度(Moderate-Intensity)スタチン」「高強度(High-Intensity)スタチン」と同じではない。このことを知らない人はまだ多数いるはずだ。
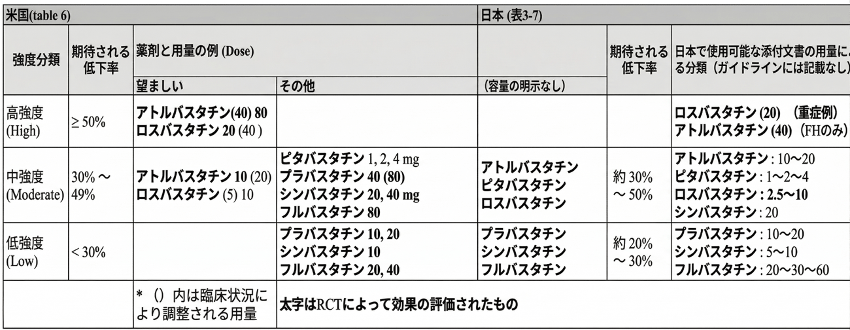
注:A Iが言うことを聞かず、上記表の太字は不適切である(薬剤と容量の分類は合っている)
日本ガイドラインにおいては以下の点に留意が必要である。
- 「スタンダードスタチン」という呼び名はガイドライン中に出てこない
- 「ストロングスタチン」という呼び名は使われているが、どのスタチンを指すかは明示されていない(!!)
- 表3-7では、LDL-C低下作用の強さに応じて2グループに分かれているが、具体的な用量は示されていない
重要:LDL-C低下率の高いグループ(アトルバスタチン・ピタバスタチン・ロスバスタチン)をストロングスタチンと呼ぶのだろうかと推測するしかない。そしてそれらは一部を除いて、ほとんどが米国の低強度・中強度スタチンのカテゴリーに分類される(正確にはガイドラインのオリジナルを参照されたい)。
日本ではストロングスタチンの使い所は二次予防でしか明言されていない。
FQ18:「冠動脈疾患の二次予防の薬物療法において最大耐用量のストロングスタチンを第一選択に推奨できるか?」
推奨文:「冠動脈疾患の二次予防においては、治療開始前のLDLコレステロールに関わらず、発症早期より最大耐用量のストロングスタチンを第一選択にした薬物療法を推奨する。」
一次予防でどのようなスタチンを使用するかは指示されておらず、LDL-Cの低下率や数値目標が明示されているのみである。
日本で行われた一次予防RCT
日本人で「ASCVD未発症者」を対象としたスタチンのRCTは、実質的にMEGA Studyのみである。前回エントリーのここにもMEGA studyについては少し記述あり。
Nakamura H, Arakawa K, Itakura H, et al; MEGA Study Group. Primary prevention of cardiovascular disease with pravastatin in Japan (MEGA Study): a prospective randomised controlled trial. Lancet. 2006;368:1155-1163.
そこで使用されたスタチンはプラバスタチン10〜20 mg/日(スタンダードスタチン:米国でいう低強度スタチン)のみである。
海外で効果の示されている一次予防用スタチン
一方、海外における一次予防の直接的な根拠が存在する薬剤としては以下が挙げられる。
| スタチン名 | 有効性が確認された主な用量 | 根拠となった代表的な試験名 |
|---|---|---|
| アトルバスタチン | 10 mg | ASCOT-LLA CARDS(糖尿病一次予防) |
| ロスバスタチン | 20 mg / 10 mg | JUPITER(20mg) HOPE-3(10mg) |
| プラバスタチン | 40 mg | WOSCOPS |
| ピタバスタチン | 4 mg | REPRIEVE(HIV陽性者) |
| ロバスタチン(日本未発売) | 20〜40 mg | AFCAPS/TexCAPS |
つまり、「外挿を極度に嫌いクラスエフェクトを信用せず、内的妥当性だけでエビデンスを採用する」ならば、日本人の一次予防で選択すべきスタチンはプラバスタチン10〜20 mg/日一択ということになる。外挿についてはこちら
LDL-C低下ありきか、スタチンありきか
これも日米で考え方が異なる。
数値目標の設定(treat to target)について
FQ16:動脈硬化性疾患の予防のため管理目標値を目指したLDLコレステロール低下療法を日本人において推奨できるか? → コンセンサス/A
コンセンサス、つまり明確な研究の根拠はない(にも関わらず推奨レベルA)。「目標値を定めて治療する群(Treat to Target)」と「目標を定めず定量を投与する群(Fire and Forget)」を直接比較したRCTやメタ解析は世界的に存在しない(それでもなぜA推奨なのかはガイドラインを参照されたい)。なお二次予防では、冠動脈疾患患者を対象としたTreat to Target(T2T)とFire and Forget(FF)を直接比較した韓国の多施設RCT「LODESTAR trial」があり、Treat to Target(T2T)は非劣性が示されている。
スタチン至上主義か、何でも良いのか
日本ではLDLを下げるのにスタチンでなくても良い、としている。
FQ20:アテローム性動脈硬化疾患の予防目的としてスタチン以外の薬剤を用いたLDLコレステロール低下療法を推奨できるか? 推奨度 1+ エビデンス A
その根拠として以下の2本が引用されている。
Silverman MG, Ference BA, Im K, et al. Association between lowering LDL-C and cardiovascular risk reduction among different therapeutic interventions: a systematic review and meta-analysis. JAMA 2016;316:1289-97.
Marston NA, Giugliano RP, Im K, et al. Association Between Triglyceride Lowering and Reduction of Cardiovascular Risk Across Multiple Lipid-Lowering Therapeutic Classes: A Systematic Review and Meta-Regression Analysis of Randomized Controlled Trials. Circulation. 2019;140(16):1308-1317.
つまり、使うべき薬物の種類は問わず、LDLが下がりさえすれば良いという考え方である。日本のガイドライン本文には「薬物を使う場合はまずスタチン」というニュアンスはどこにも見られない。(ただし、発行学会のガイドラインの別途概説記事では「Of the various antilipid medications, statins remain the recommended first-line drugs for lowering LDL-C levels.」という表現がなされている https://www.jstage.jst.go.jp/article/jat/31/8/31_RV22019/_html/-char/en )。
前回のエントリーで「スタチンなしで、それ以外の薬しか使われていない患者さんの主治医の処方ロジックを聞いてみたい。」と書いたが、それらの先生方は日本の推奨に忠実に従っていたに過ぎない。
一方、米国(2026)はTable 5のスタチンの欄において以下のように記述している。
First-line therapy for ASCVD risk reduction in nearly all patients
また本文でも以下のとおりである。
Numerous cardiovascular outcome trials (CVOT) have demonstrated safety, tolerability, and efficacy for both LDL-C lowering and ASCVD risk reduction, justifying statins as the cornerstone of pharmacotherapy to lower LDL-C and risk of ASCVD events
ここは明らかな日米の齟齬であり、どっちを取るか、ではなく、両方のガイドラインの要求を満たしたいならばスタチンを第一選択とするのが無難である(それ以外の薬剤のみで治療している場合、日本の推奨は満たすが、米国の推奨からは逸脱していることになる)。
この見解の相違は、かなり質問の方法を変えながら複数のAIと議論したが、両方の立場の違いを綺麗に説明する理屈には辿り着けなかった。(私見としては、やはり相当の理由がない限りスタチンfirstであるべきと考えている)
目標値の設定についての考え方の違い
日本の目標値、治療閾値はどこから来たのか
2%および10%という閾値の設定根拠
吹田スコアは欧米のスコアのように脳卒中のリスクを含んでいなかった。またLDL-Cがスコア算定に含まれるのが吹田と久山町のみであり、吹田スコアは改訂版では140 mg/dL以上か未満かのの二値だったが久山町は段階的だった。脳卒中を含むことも理由となり、久山町スコアが採用された。
Kokubo Y, et al. Development of a cardiovascular disease risk prediction model using the Suita study, a population-based prospective cohort study in Japan. J Atheroscler Thromb. 2020;27(7):739–751.
久山町研究ではLDL-Cが120 mg/dL未満(基準)・120〜139 mg/dL・140〜159 mg/dL・160 mg/dL以上に分類されており、その基準値は2017年版の管理目標値に沿った値となっていた(120 mg/dL未満をreferenceとしていた)。
Honda T, Chen S, Hata J, et al. Development and validation of a risk prediction model for atherosclerotic cardiovascular disease in Japanese adults: the Hisayama Study. J Atheroscler Thromb. 2022;29(3):345-361.
【重要】 米国(後述)ではリスクベネフィットの拮抗点を厳密に治療閾値とするのと異なり、この「2%」や「10%」という数値自体に特定の生物学的な臨界点があるというよりは、日本人の一般住民集団(久山町研究のコホート)において、リスクが高い人(上位20%)と低い人(下位35%)を分けたという説明が最も合理的(20%。35%となるようなカットオフを調べたたら2%、10%だった、なのか2%、10%と決めたら、たまたま20%。35%となったのかは不明。上記Hondaらのfig1の脚注に記載あり)
さらに、
吹田スコア(脳卒中を含まない)の2%・10%のカットオフと、久山町スコア(脳卒中を含む)の2%・10%のカットオフで集団分布が大幅に変わらないため、それをカットオフとしよう、という論理である。
絶対リスクのグレードの設定は、久山町研究において10年以内の動脈硬化性心血管疾患(冠動脈疾患とアテローム血栓性脳梗塞)発症確率が 2%未満を低リスク、2%以上10%未満を中リスク、10%以上を高リスクと設定しており、本ガイドラインではその値を採用した。(中略)
絶対リスクは、研究対象となる集団の年齢構成やアウトカムの把握方法の違いによって左右されるが、この基準による管理区分による各リスク群の割合は2017年版の本ガイドラインの管理区分とほぼ合致した
低下率なのか目標数値なのか
米国ではLDL-Cの低下率を治療の第一目標(target)としているが、日本ガイドラインには以下の記述がある。
「わが国における実臨床の場では管理目標があるほうが患者のアドヒアランスの観点から望ましく、実際に多くの実地臨床家が管理目標値を見て治療の目安にしていることから、従来通り管理目標値を維持するべきである」(2017年版から引き継ぎ)
管理目標値の決定については
LDL-Cの管理目標値は、観察研究および介入研究のシステマティック・レビューによって決定された。高リスク管理区分では120 mg/dL未満とし、低リスク・中リスク管理区分では2017年版ガイドラインの管理目標値を引き継ぎそれぞれ160 mg/dL未満、140 mg/dL未満とした
と記されているが、「観察研究および介入研究のシステマティック・レビューによって決定された」の部分に出典を示す文献番号は振られていない【重要】(2022版)
120 mg/dL未満はどこから来たか
ということで、2017年ガイドラインまで遡ると、
CQ22. Is an LDL-C management target of <120 mg/dL appropriate for high-risk category of primary prevention?
• The LDL-C level for high-risk patients in primary prevention should be controlled at a target of <120 mg/dL.(Evidence level 2, recommendation level B)
Evidence level 2 = 前向きコホート研究・そのMA/SR・(事前規定された)RCTサブ解析 Recommendation level B = 弱い推奨
上記推奨の解説箇所に引用されている研究はAPPROACH-J , J-LIT, HOPE-3 studyの3本で、以下の3点を根拠にLDL-C<120の推奨の根拠としている。
1)APPROACH‑Jは、日本人の高リスク一次予防患者を対象に、スタチン開始後2年間の心血管イベントを前向きに追跡した研究で、LDL‑Cが約120 mg/dL以下で冠動脈疾患リスクが頭打ちになる
2) J‑LITの糖尿病サブ解析では、高リスクに分類される糖尿病患者でLDL‑C<120 mg/dLを維持することがCAD予防に有用と報告。
3) HOPE‑3試験では、日本の高リスクに相当する中等度リスク集団を対象にした一次予防RCTで、ベースラインLDL‑C約128 mg/dLの被験者にロスバスタチンを投与し、LDL‑Cを120 mg/dL未満(実際には90 mg/dL台)に下げた群で有意な心血管イベント減少が認められた
上記をAIにそれぞれの論文の出典をもとにファクトチェックをかけると以下の理由で「やや“盛って”いる」と判断される。
一次論文ベースで厳密に言い直すなら:
• APPROACH‑J: 高リスク一次予防日本人で、スタチンによりLDLを120 mg/dL前後まで下げている群でイベントが少ない、という観察データはあるが、「120でリスクが頭打ち」とまでは言えない。ここはガイドライン側の表現がやや盛り気味と評価せざるをえない• J‑LIT糖尿病: 糖尿病(高リスク)では、治療中LDLが低いほどCADが少なく、カテゴリー解析から「120未満」が一つの目安とはなりうるが、cutoffとして検証したわけではない。→ 方向性はエビデンスと合っているが、「120という数字そのものが検証された」かのようなニュアンスは一段階盛っていると言える
• HOPE‑3: ベースライン約128 mg/dLの中等度リスク者が、スタチンで約90 mg/dL台まで下がり、イベントが有意に減った。→ ここは、元のHOPE‑3の結果を「120未満」という数字に“引き寄せて”説明しており、事実よりかなり簡略化・圧縮されているこれらは「120より低いLDLでも有効・安全」という間接的根拠にはなるが、「120ちょうど」を検証した試験ではない。このように、「120 mg/dL」は、これらのエビデンスを踏まえてガイドラインが置いた実務的なコンセンサス値であって、「3本の試験が120という閾値そのものを直接証明した」とまでは言えない、「複数の研究で得られた“低ければ低いほどよい”傾向を、日本の現場向けに120という実務的なターゲットにまとめ直した」 という性格の文章。「2017ガイドラインの当該記述は、一次論文の結果を土台にしつつ、LDL‑C<120 mg/dLという目標値を正当化する方向にやや強めに要約している(盛っている)」
付記:
APPROACH-J: 全員プラバスタチン内服の観察コホート。結果的にLDLがどのぐらいだったかによってLDL-C level を4分位に分けて(Q1, ≤ 104.9 mg/dL; Q2, 105.0 to < 119.0 mg/dL; Q3, 119.0 to < 133.0 mg/dL; and Q4,≥ 133.0 mg/dL)アウトカムを見たら、「直線状に(プラトーなし)」達成LDLが低いほどイベントが少なかった。
HOPE-3:ランダム化期間の中央値は5.6年、プラセボ群のイベント発症率(ASCVD)4.8%、ざっくりとした近似で8〜9%程度(厳密計算でも8%台)対象患者の内訳中国人30%、南アジア15%。
J-LIT はフルテキストにアクセスできず。
まとめ:120 mg/dL未満についてはEvidence level 2, recommendation level Bとして文献も引用されているが、その文献をきちんと読むと、120 mg/dL未満の目標にすべし、という結論に辿り着くようには思えない。
160 mg/dL未満、140 mg/dL未満の科学的根拠はない
さらに、2022版で「低リスク・中リスク管理区分では2017年版ガイドラインの管理目標値を引き継ぎ」とあるが、2017年版のガイドラインを隅々まで読んでも160 mg/dL未満、140 mg/dL未満の根拠となる研究や考え方はどこにも明示されていない【重要】
ここまでをまとめると、「国内データ(久山町)で作った10年ASCVDリスクスコアを採用し、そのリスク区分とLDLカテゴリが、従来の吹田スコア/2017年ガイドラインとほぼ同じ集団割合・数値になるように調整し、社会的混乱を避けることを優先し踏襲した」という、いかにも日本らしい明確な科学的根拠のないリスク分類のカットオフおよび、数値目標の設定である。
(まあ吹田スコアで低リスクだった人が、ガイドラインが変わって久山町スコアでやったら高リスクに再分類された(ので急に治療方針がガラッと変わる)、みたいなことはない方が良い、というロジックは理解は可能ではある)
米国の治療閾値の設定
米国の中強度スタチン開始のカットオフは、新規発症糖尿病(NODM:new onset DM)の発症とASCVD抑制効果とのリスクが釣り合うところ(拮抗点)で、中強度スタチンは約3%である。「奇しくも」CTT collaborationというメタ解析でのプラセボ群のイベント発生率が10年で3%に相当する。
日本での治療開始閾値を米国式で考える(ようやく本エントリーの本題)
介入の判断基準となる拮抗点では、「スタチンによる10年間のイベント抑制効果(絶対リスク減少)」と「10年間の新規糖尿病発症リスク(絶対リスク増加)」が等しくなる必要がある。
10年間のベースラインリスクを R10、スタチンによる相対リスク減少率を RRR、糖尿病の絶対リスク増加分を ARI(DM)とすると、以下の平衡式が成立する地点である。
R10 x RRR = ARI(DM)
これをR10に対して解くと、ベネフィットがハームを上回り始める境界線となる10年ASCVDリスクR10は以下のとおりとなる。 R10 = ARI(DM)/RRR
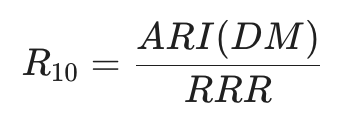
治療効果(MEGA Study)
MEGA studyは日本人対象唯一の大規模一次予防RCTとして、プラバスタチン10〜20 mg/日(米国的には低強度)の効果を7,832例で検証した。
Nakamura H, Arakawa K, Itakura H, et al; MEGA Study Group. Primary prevention of cardiovascular disease with pravastatin in Japan (MEGA Study): a prospective randomised controlled trial. Lancet. 2006;368:1155-1163.
| エンドポイント | 追跡5.3年 ARR | NNT(5.3年) | NNT(10年外挿) |
|---|---|---|---|
| 冠動脈疾患(CHD) | 0.84%(95%CI 0.2〜1.5) | 119 | 約64 |
| CHD+脳梗塞(複合CVD) | 3.6% vs 2.5% | 91 | 約50 |
拮抗点のためのR10やRRRを算出するには米国や久山町リスクであるASCVDで二次エンドポイントの「全心血管イベント(All cardiovascular events)」を指標とした数値で行う必要がある。
対象: 冠動脈疾患(CHD)+すべての脳卒中(脳梗塞、脳出血、分類不能)+その他すべての心血管死。
データ: 食事療法群 8.5 / 1000人年 vs プラバスタチン群 6.4 / 1000人年。
10年換算: 1000人年あたりの数値を10倍するため、そのまま 8.5% vs 6.4% 。
NNT=48, RRR=0.26となる
この研究では対象患者は吹田スコアや久山町スコアでのリスク分類の分布は記されておらず、だいたい一次予防の低〜中リスク層中心という位置づけ。→ 実際にどのぐらいのリスクのグループだったかは、前回のエントリーで解説(計算上は1.4%だったが実質的には10年リスク約8.5% ぐらいの集団)
ただし、バイアスの多さは指摘されていて、
* 前向きランダム化比較試験だが、二重盲検ではなくオープンラベル
- → パフォーマンスバイアス/検出バイアスが入りやすい
- → エンドポイントの一部がソフトで、判定に主観の入る余地がある
- → 食事療法が両群で異なる形で運用されうる(実臨床寄りの「複合介入」)
* イベント数が比較的少なく、推定値が不安定になりやすい
などがあるが、他に根拠とできる研究が存在しないため、これでやるしかない。
まとめ:実質10年リスク約8.5% ぐらいの集団でNNT=48, RRR=0.26
日本人でのスタチンによる糖尿病発生率
Yamazaki K, Takahashi Y, Teduka K, Nakayama T, Nishida Y, Asai S. Assessment of effect modification of statins on new-onset diabetes based on various medical backgrounds: a retrospective cohort study. BMC Pharmacol Toxicol. 2019 May 28;20(1):34.
日本人コホートによる補完データとして、Yamazaki(日本人1,000例、propensityスコアマッチング)では10年のDM絶対リスク差(ARI)が6.0%(スタチン群15.6% 対 非使用群9.6%)、つまりNNH=17と報告されている。これは観察研究の限界(confounding by indicationや検査バイアス)を反映して、RCTより若干低い値を示す。NNH 17という値は、欧米RCTメタ解析(Sattar 2010)の NNH 255 と比べて格段に小さく見える。これは①高リスク患者が集まる大学病院コホートという選択バイアス、②検出バイアス(スタチン服用者の検査頻度が高い)、③残余交絡の影響が大きいと著者自身も考察している
この研究で使用されたスタチンは、アトルバスタチン(N=121)・フルバスタチン(N=24)・ピタバスタチン(N=70)・プラバスタチン(N=71)・ロスバスタチン(N=110)・シンバスタチン(N=18)・2種類以上(N=86)である。(投与量の記述はなく、スタンダードスタチンとストロングスタチンが混在している)
スタチンを入れると1人の利益あたり3人の害
つまりMEGA集団のベースライン10年CVDリスク約8.5%の集団を48人治療すると、しない場合に比べて約1名余分にASCVDを減らす代わりに、約3名弱(17×3≈51)の新規糖尿病患者を発生させる。治療に見合わないということである。
「糖尿病を3人発生させてもASCVD 1例予防する意義はあるのではないか」という主張はあり得るが、それを認めると米国の治療閾値の設定の議論自体意味がなくなる。
拮抗点の計算
では利益と害が拮抗する10年ASCVDリスクはどこなのか?(MEGA studyでのCHD+脳梗塞(複合CVD)のスタチンによるHR=0.74を使用)
R10 = ARI(DM)/RRR= 0.06/0.26=0.23 (ARI(DM)=0.06は前述の6%から)
10年ASCVDリスク23%以上の場合のみ、スタチンによる治療の利益が害を上回る。久山町スコアとの対応は以下のとおりである。
- 60〜69歳(およびそれ未満):最大の19点でも10年リスク22.9% (<23%)で治療閾値を超えない
- 70〜79歳:15点前後で10年リスク25.9%%に相当 (14点だと22.9% <23%)
ただし、Yamazakiは日本人実臨床のデータだが観察研究であり、サーベイランス・交絡バイアスが含まれる(NNHを小さく見積もる=リスクを大きく見積もる)。
NNH=34(リスク半分)と仮定した場合(半分と仮定する根拠はない):
R10 = ARI(DM)/RRR= 0.03/0.26=0.115 (11.5%)
また、日本のガイドラインでスタンダードスタチンの対象となる10年ASCVDリスク2%が治療と害の拮抗点になるために必要なARI(DM)は上記同様逆算すると0.5%(つまりNNH(10年)は200)となる。Yamazakiの研究では非使用群の10年リスクが9.6%であることから、「非使用9.6% vs スタチン10.1%」という比較になる。
ピタバスタチンと糖尿病リスク
NODMのリスクを上げないスタチンが存在するなら、上記のような治療閾値の設定は不要で、程度の差はあれ、全ての人がスタチンによる恩恵を得ることができるはずである。
ピタバスタチンは糖尿病のリスクを上げない(むしろ下げる)とされている。
J-PREDICT試験(ピタバスタチンの介入試験):耐糖能異常(IGT)を有する日本人1,269名を対象としたRCTで、他のスタチンとは対照的に、ピタバスタチンの投与は生活習慣改善群と比較して糖尿病への移行を18%抑制した(HR 0.82)と報告されている。
REAL-CAD試験のサブ解析:安定冠動脈疾患患者約1.3万人を対象とした試験で、ピタバスタチン1 mg(低用量)と4 mg(高用量)を比較した際、3.9年間の追跡で新規糖尿病発症率に有意な差は認められなかった(4.5% vs 4.3%, p=0.76)。
NNDが無限大であれば、理論上誰に対するスタチン投与も(原則)正当化される。ならばピタバスタチンを使えばいいではないか、といいたいところだが、J-PREDICT試験は「IGT患者」のNODMをメインアウトカムとした一次予防試験であり、副次評価項目の心血管イベントには有意差がなく、糖尿病は増やさないものの本来の目的であるASCVDの予防効果が示されていない。(REAL -CADは安定冠動脈疾患患者対象の二次予防のため適用できない)
脳卒中増加リスクについて(余談)
欧米で行われた高用量スタチンを用いた二次予防試験(SPARCL試験)では、脳梗塞を減らす一方で脳出血が有意に増加した(ハザード比1.66)と報告されている。日本の脳卒中は脳出血の比率が海外より多いため、この副作用は懸念となる。しかし日本人を対象としたJ-STARS試験やMEGA Studyのサブ解析においては、スタチン投与によって脳出血リスクの上昇は認められていない。
J-STARS(Japan Statin Treatment Against Recurrent Stroke)は、日本人脳梗塞既往例におけるプラバスタチンによる脳卒中再発(二次予防)試験である。結論として、日本人においてスタチンが脳内出血のリスクを高めることなく、特にアテローム硬化が関与する脳梗塞(アテローム血栓性脳梗塞)の予防に寄与することを証明した試験といえる。
J-カーブ現象は存在するのか(余談の余談)
これも丁寧に議論をするととても長くなるので端的に。
相関研究でLDL-Cが低いほど脳出血が増える、という結果や総死亡が増えるという結果(J ~LIT)などがあるが、RCTでは前述のJ-STARSも含めthe lower, the betterであり、「観察研究でのJ-カーブ現象は主に逆因果関係によるもの:そもそもの重篤な疾患や衰弱状態が低LDL-Cと死亡率上昇の両方を引き起こしている可能性が高い」(perplexity, consensus, open evidenceの出力を総合)と考えるので良さそう(これも時間があれば深掘り予定)
日本のガイドラインにおいても若干の言及はあり、「日本の疫学調査では、LDL-Cが 80 mg/dL 以下になると脳出血の頻度が増加すると報告されている。ただし、臨床試験のメタ解析では「薬物療法による低下」が直接脳出血を増やしたという明確な証拠はないため、出血リスクを評価した上での適切な管理が推奨」とされている。
Therefore, appropriate LDL-C lowering therapy should be implemented after assessing bleeding risk as well.
これを踏まえて脂質異常症のスクリーニングは誰を対象にすべきか
仮に、一度も検診や医療機関で脂質を測定されたことのない個人がいたとする(いないかもしれないが)。その人に資質の検査(スクリーニング)をすべきか? という問いにいは、
70歳までは久山町スコアが何点であってもスタチンの適応とはならない(最大ポイントでも23%を超えることがない)ためスクリーニング不要と考えられる。
- 70〜79歳:15点前後で10年リスク25.9%%に相当 (14点だと22.9% <23%)
脂質測定の結果から加算されうる点数は、最大5ポイントのため、脂質スクリーニング検査のカットオフ(脂質の結果を除く久山町スコアの合計)は以下のとおりとなる。
- 70歳まで:スクリーニング不要
- 70〜79歳:10点以上
10年リスク23%・NNH =17の違和感
ここまでを読んで違和感を抱いた人は多いかもしれない。米国と同じ利益とNODMの拮抗点でスタチンの投与閾値を決めるという理屈から行くと日本人での一次予防の治療閾値は10年リスク23%を超える必要がある、というのはその通りだが、それ未満のリスクではスタチンが推奨されない、と言われても米国が3〜5%を超えたら中強度スタチンを検討というのと比べると、罹患率が3倍の違いということを考慮しても違和感は拭えない。
この違いは、投与閾値の計算根拠となるスタチンのNNHの違いからきている。米国の中強度スタチンの投与閾値の計算はNNH=100をもとにしており(Satter, Newman)、日本はYamazakiのNNH=17をもとにしている。(日本人は海外よりスタチンによるNODMのリスクが6倍近いというのも違和感が拭えない)
では日本人のスタチンによるNODMの研究は他にないのか?というともう1本だけ存在する
Ooba N, Setoguchi S, Sato T, Kubota K. Lipid-lowering drugs and risk of new-onset diabetes: a cohort study using Japanese healthcare data linked to clinical data for health screening. BMJ Open. 2017 Jun 30;7(6):e015935.
が、
- 平均追跡期間は 1.96年と短い
- 観察コホートであり、無作為化されていない(スタチン開始群は、元々メタボ・高血糖・肥満などのリスクが高い人が選ばれやすい(confounding by indication)
- 短期特有の過渡現象(surveillance・治療開始バイアス)がそのまま反映されたARIになってしまう
- それを単純に「×5して10年ARI」として使うと、長期リスクの推定としては信頼できない
という理由から、10年のNNHを算出するには適さない。
類似の民族である東アジアでの研究は3本(Lee et al. Ther Clin Risk Manag. 2016(韓国), Chung J, et al. Sci Rep. 2023(韓国), Lin et al. J Atheroscler Thromb 2022(台湾))あるが、韓国の2本はどちらも冠動脈疾患を有する患者の二次予防、Chung, Linの2本はプラセボ群が存在しないため算出不可能。二次予防も含めて良いとすれば、Leeは算出可能だが、1.93%/年→ 19.3%/10年→ NNH=5とさらに違和感の大きい数字となる。(上記Oobaと同様の理由)
余談ではあるが日本で唯一のスタチンによる一次予防研究であるMEGA studyのサブ解析でもNODMを調べている。しかし、 172/3013 (5·7%) vs 164/3073 (5·3%) OR 1·07 (0·86–1·35) と有意差は出ていない。(だから閾値は存在せず、害を気にせず遠慮なく投与して良い、ということではない。サブエンドポイントのため、βエラーの可能性がある+幾つものメタ分析で、スタチンによるNODMの害の存在は認められており、ほぼ間違いないと思われる)
海外とNODMのリスクが同じならば治療閾値はどうなるか?
日本人も欧米人もスタチンによるNODMの発症リスクは同じはずだから、海外の文献で考えれば良いのではないか? と仮定するとどうなるか。
米国の3%のカットオフに用いられる中強度スタチンのNNH=100は
Sattar N, Preiss D, Murray HM, et al. Statins and risk of incident diabetes: a collaborative meta-analysis of randomised statin trials. Lancet. 2010;375(9716):735-742.
からきている。(これは14本の一次予防RCTのメタ解析で、実はMEGA studyも含まれている)これと同じ数字を採用するなら、治療閾値は米国と同様の3%がカットオフである。
現時点で最新最大のスタチンによるNODMのメタ解析は
Reith C, Blackwell L, Emberson J, et al; Cholesterol Treatment Trialists’ (CTT) Collaboration. Effects of statin therapy on diagnoses of new-onset diabetes and worsening glycaemia in large-scale randomised blinded statin trials: an individual participant data meta-analysis. Lancet Diabetes Endocrinol. 2024;12(5)306-319.
で、NNH=84とされている(二次予防の研究も含む)
1次予防に限定したメタ解析は
Finegold JA, Manisty CH, Goldacre B, Barron AJ, Francis DP. What proportion of symptomatic side effects in patients taking statins are genuinely caused by the drug? Systematic review of randomized placebo-controlled trials to aid individual patient choice. Eur J Prev Cardiol. 2014 Apr;21(4):464-74.
で、この研究の4年NNH=200から10年換算するとNNH≈80となる
これらを踏まえて(おおむねNNH=80~100だが、安全サイドでの80を採用)治療拮抗点を計算すると、
R10 = ARI(DM)/RRR= 0.0125/0.3=0.416 ≈ 4.2%
もう一つの懸念:低リスク群のスタチン投与は意味がないかもしれない
これについてのロジックをここで詳細に書くと本記事の同じかそれ以上の長さになり得るので、先に以下にまとめておいた。
ここに転記はしないのでせめて上記の「まとめ」だけでも参照されたい。
以上を踏まえて日本のガイドラインとその周辺について言えること
ガイドライン
- 日本人の心血管リスク推定は久山町スコアがベスト(しかしオリジナルからガイドライン版への飛躍があり、そこの正当性は検証されていない)
- 低、中、高リスクを分けるための2%および10%という境界ラインの根拠は科学的ではない(下から集団分布が35%、45%、20%になるように分けた、ということだがその根拠が不明。せめて両端標準偏差の1倍とか2倍で切るではダメなのか?)
- 高リスク群の一次予防の目標 LDL-C<120は根拠論文が提示されているが、そこのロジックはあまり厳密ではない
- 低、中リスク群の治療目標160 mg/dL未満、140 mg/dL未満の科学的根拠はない
その周辺
- 日本人の一次予防のRCTはMEGA studyのみ。おおむね中リスク患者(10年リスク約8.5%)、使われたのはプラバスタチン10~20mgのみ (ガイドラインが推奨している2%〜8.5%のリスクの患者にはエビデンスが存在しない)
- 日本人におけるスタチンのNODMのリスクを10年NNHとして推定できるのはYamazakiの研究のみ(NNH=17)だがコホート研究やその他のバイアスによりNNHは過剰評価に出ている可能性 この数字を使うと治療の利益が害を上回る拮抗点の10年リスクは23%
- ピタバスタチンはむしろNODMのリスクは減らすが、そもそも肝心なASCVDに対する一次予防のエビデンスが日本人で存在しない。
- 日本人におけるスタチンのNODMのリスクが他の人種と同じぐらいと仮定するならば治療閾値のカットオフ10年リスクは4.2%
- しかしながら低リスク群での一次予防はそもそもASCVD予防の効果があるかははっきりしていない。(これは議論がある。米国のガイドラインはどれだけベースラインリスクが小さくてもスタチンのASCVDを減らす効果は存在し、NODMとのバランスだけで治療閾値を決めればよい、というスタンス
結局どうすれば良いのか?
日本のガイドラインが「@#%&!だ」と書いたが、ひいき目に見るなら、厳密な科学的根拠に基づいて作成したかったが、海外のものを、そのまま流用することはできない(罹患率が異なるために)。一方、根拠とするための日本人の研究がすくなすぎる(ほぼない)ために、理論的に決めることは不可能で、「現実的に、覚えやすく、運用しやすいこと」を優先として、えいやっと決めるしかなかったのだろう、と思う(極めて日本的だが)。
ここまでの議論のとおり、論理だけでどこからも文句の出ない方針を決めることは難しい。
取りうる選択肢は大きく4つ。どれがベスト、とは言い難く、あちらを立てればこちらが立たず、でどれも一長一短。
| 選択肢 | 一次予防のスタチン投与閾値(10年リスクで) | 一次予防のスタチンと用量 | メリット | デメリット |
| 全て日本のガイドライン通り | 2% | 日本で認められているすべてのスタチンと用量(またはスタンダードスタチン) | 日本のほぼすべての医師の診療から逸れないため、誰からも咎められない | エビデンスに(かなり)基づかない医療 |
| (外挿をせず)日本のエビデンスだけで言えることのみに基づく | 23% | プラバスタチン10−20mg | ・最も厳格なエビデンスの適応 ・自分の診療が最も厳格なエビデンスに基づいているという満足感 ・低リスクグループにはスタチンの効果がない/または有害かもしれないという部分を尊重できる(日本の研究はないが) | ・たった2本のバイアスリスクの高い研究が根拠 ・直感的に違和感(日本人の大半が一次予防の対象から外れる) ・多くの本来治療すべき人を治療せず機会損失となるかもしれない |
| 米国のガイドラインの閾値の「考え方」に基づいて独自に設定 | 4.2% | 上記+ アトルバスタチン 10 mg ロスバスタチン 10 mg | 治療閾値は「感覚的に」合理的と思える(海外と同じNODMリスクと考えるので、カットオフも類似する) | ・一次予防で最初からストロングスタチンを使用 ・LDL-Cが下がりすぎるリスク ・低リスクグループにはスタチンの効果がない/または有害かもしれない(のに治療してしまうリスク) |
| 全て米国のガイドライン通り | 3% | アトルバスタチン 10 mg ロスバスタチン 10 mg | 一応現存の最新のエビデンスに則った診療と言える | 日米の疫学の違いを考慮していない(ため過剰治療になるリスク) |
注:アトルバスタチン 10 mgとロスバスタチン 10 mg の根拠は海外で効果の示されている一次予防用スタチンによる
上記4案の他にはMEGA studyでは効果は証明され、害は生じていない、という観点を重視するなら、その対象の平均的な10年リスク約8.5%を超える事例は予防投与して良い、という立ち位置もあると思う。
これらを踏まえて、「私案」として(かなり根拠はないが、根拠のなさは日本のガイドラインと同じぐらいだと思う)
カットオフ
スタチンを「検討」:10年リスク4.2%(世界の知見を踏まえる) で、使用する場合はNODMの発現のリスクを説明の上、注意深くモニタリングとセット
スタチンを「提案」:10年リスク15%または20%(どちらかに決める十分な根拠もないので、どちらでも良いと思う)
使用すべきスタチンと目標
プラバスタチン10mgまたは20mgがファーストチョイス。LDL-Cの低下率が少なくとも30%超えを目指す(160→112, 150 →105, 140 →98のイメージ)、達成しない場合のセカンドラインはアトルバスタチン 10 mgまたはロスバスタチン 10 mg
ぜひ、日本のガイドラインよりもエビデンスを踏まえて、上記よりも納得感のある提案のある方は教えていただけると嬉しい。
おわりに
スタチンを適切に使う、ということがいかに難しいのか、ということがわかっていただけたのではないかと思う。
このややこしさを解決するには、
- ガイドライン版の久山町スコアとオリジナル版久山町スコアの一致度の検証
- 日本人においてのスタチン使用でNODMが実際にどのぐらい発生するのか、の本当の値
- プラバスタチン以外(MEGA study以外)での日本人でのスタチンによる一次予防のエビデンス(できればプラバスタチン以外)
- 次回の日本のガイドライン改定において(もしくは改訂を待たずに)
- 米国のガイドラインについての日本での考え方(何らかのステートメント)への言及
が早急に必要である。
ここまで




コメント